Tratamiento con 131I en Cáncer de Tiroides
Dr. Hans Bowles
1. RADIOFÁRMACO
- 131I-Na. Presentación en cápsula.
-
Mecanismo de acción:
- El 131I es un emisor beta (energía media 0.192 MeV), emisor gamma de 364 keV y vida media de 8.02 días.
- El ión yoduro se incorpora mediante transporte activo a través del symporter sodio-yodo (NIS) en la membrana basal de las células foliculares tiroideas.
- El yoduro es oxidado e incorporado a residuos tirosilo de la tiroglobulina y de las hormonas tiroideas.
2. INDICACIONES
- Carcinoma diferenciado de tiroides:
- Ablación de restos tras tiroidectomía total en riesgo intermedio o alto. Considerar en bajo riesgo para optimizar seguimiento con tiroglobulina (Tg).
- Tratamiento de tumor residual o metástasis captantes de yodo no susceptibles de cirugía.
- Tratamiento adyuvante ante sospecha de micrometástasis postquirúrgicas.
- Tratamiento empírico con Tg persistentemente elevada sin lesiones localizadas.
- Reestadificación para establecer yodosensibilidad o resistencia.
- Indicación de PET-TC con 18F-FDG en sospecha de yodorrefractariedad.
- La cirugía es el tratamiento de elección en adenopatías o metástasis resecables.
3. CONTRAINDICACIONES
- Absoluta: Embarazo (test obligatorio previo).
- Lactancia: Suspensión definitiva.
- Precaución en depresión medular, insuficiencia renal, enfermedad pulmonar restrictiva o metástasis en SNC con riesgo de efecto masa.
4. PROTOCOLO
4.1 Preparación del paciente
- Consentimiento informado y explicación de efectos secundarios y normas de radioprotección.
- Retirar compuestos ricos en yodo 15–30 días antes.
- Conocer valores basales de TSH, Tg y ATg.
- Estimular TSH > 30 mUI/ml:
- Retirada de T4 durante 4 semanas (opcional T3 inicial).
- TSH recombinante: 2 dosis de 0.9 mg i.m. separadas 24 h.
- Ingreso hospitalario si actividad > 30 mCi.
- Test de embarazo negativo.
5. BIBLIOTECA DE IMÁGENES
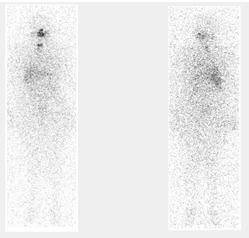
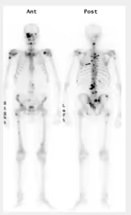
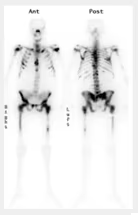
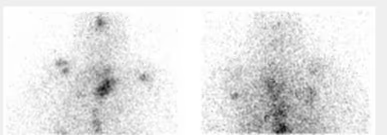
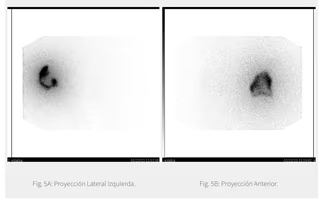
Fig. 1: Imagen planar anterior y posterior al 7° día tras dosis ablativa. Captación cervical compatible con remanente tiroideo.
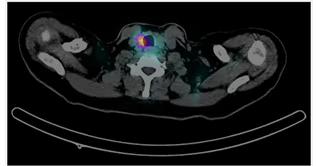
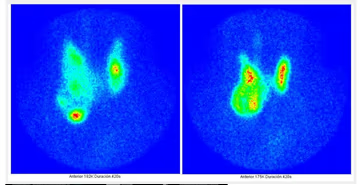
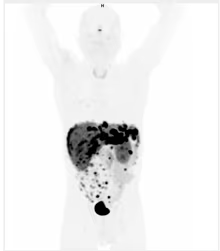
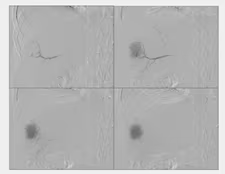
Fig. 2: SPECT-TC demostrando foco radiocaptante en lecho tiroideo derecho.
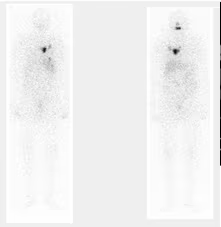
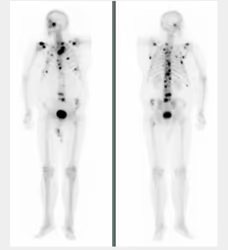
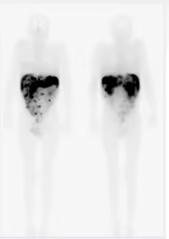
Fig. 3: Imágenes planares con focos torácicos sospechosos de metástasis.
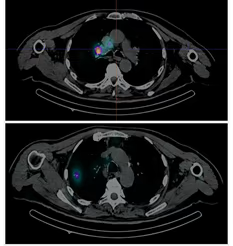
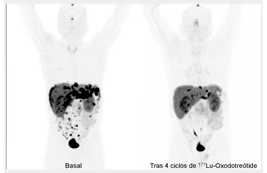
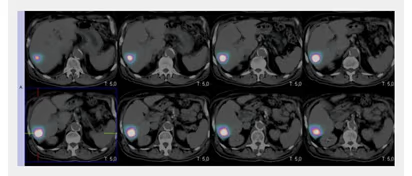
Fig. 4: SPECT-TC localizando adenopatías mediastínicas y nódulo pulmonar derecho.
6. INFORME AL CLÍNICO
- Datos del paciente y objetivo del tratamiento.
- Tipo tumoral, estadio TNM, valores de Tg y ATg.
- Tipo de estímulo TSH utilizado.
- Actividad administrada.
- Descripción de hallazgos e impresión diagnóstica.
- Recomendaciones de seguimiento y medidas de radioprotección.