Tasa de Filtración Glomerular
Dr. Hans Bowles
1. Radiofármaco
- Disolución de edetato de cromo (51Cr-EDTA). Actualmente no disponible en España.
- Disolución de pentetato de tecnecio (99mTc-DTPA).
2. Tipo
- Radiofármaco listo para su uso: 51Cr-EDTA.
- Preparación extemporánea: 99mTc-DTPA.
3. Indicaciones
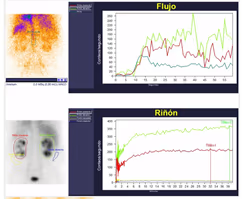
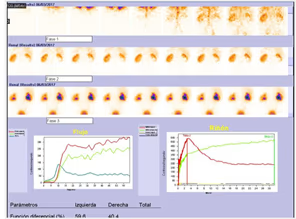
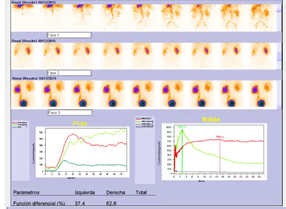
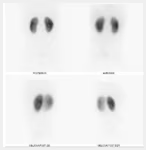
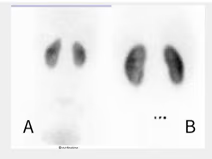
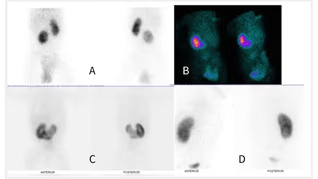
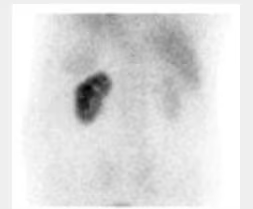
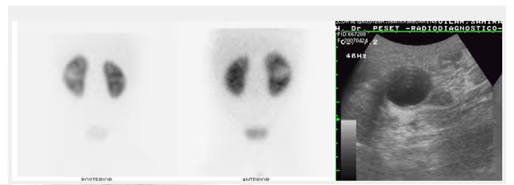
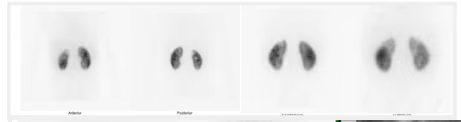
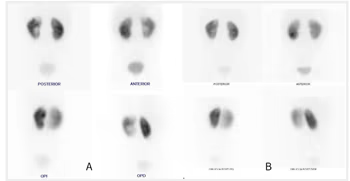
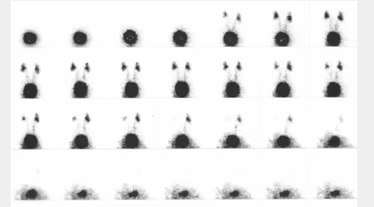
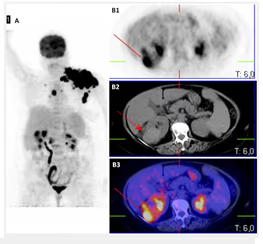
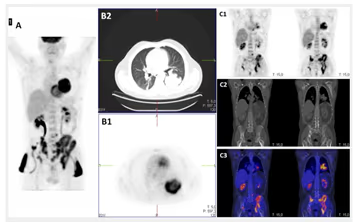
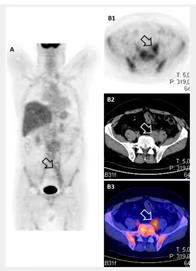
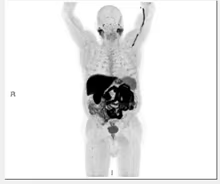
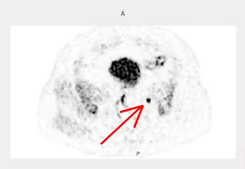
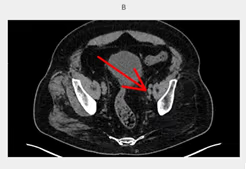
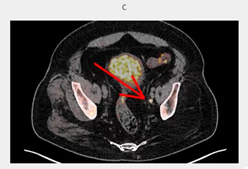
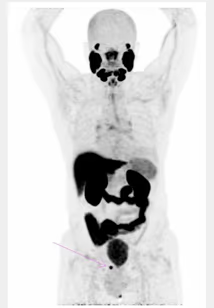
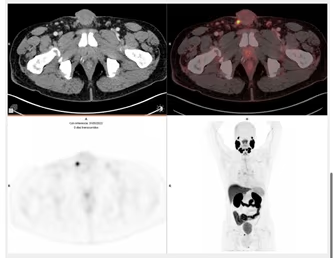
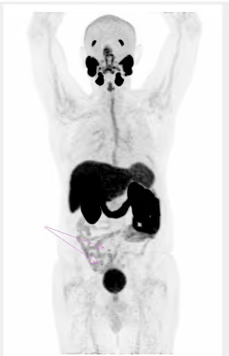
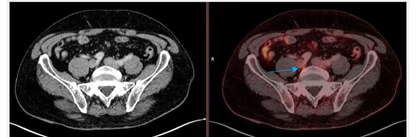
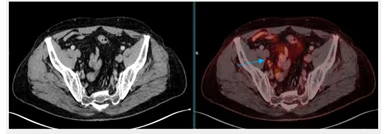
- Estudio de la función renal.
- Determinación de la tasa de filtración glomerular (GFR).
4. Procedimiento
- El paciente debe estar bien hidratado.
- Colocar vía en un brazo y extraer 5 ml de sangre (muestra basal).
- En brazo contralateral administrar:
- 80 µCi de 51Cr-EDTA, o
- 1,8–3,7 MBq de 99mTc-DTPA.
- Extraer 5 ml de sangre a los 5, 10, 20, 120, 180 y 240 minutos.
- Preparar un estándar del radiofármaco administrado.
- Centrifugar muestras y separar plasma.
- Contar actividad del estándar y de las muestras plasmáticas.
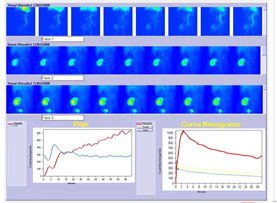
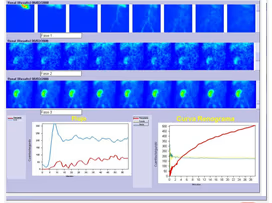
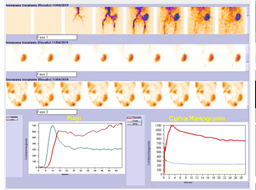
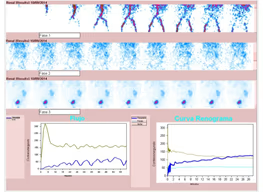
5. Cálculos
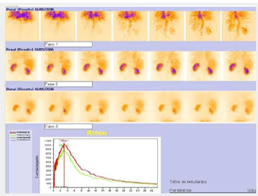
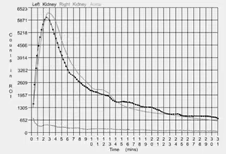
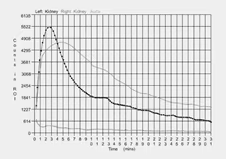
- Representar actividades del estándar y muestras plasmáticas en función del tiempo.
- El denominador corresponde al área total de aclaramiento plasmático bajo la curva.
- A y B: intersecciones de las exponenciales en tiempo cero.
- A1 y A2: constantes de las dos exponenciales.
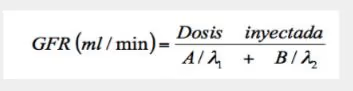
6. Valores de Normalidad
- Referidos a superficie corporal estándar de 1,73 m².
- Valor normal aproximado: GFR = 120 ml/min.