VENTRICULOGRAFÍA ISOTÓPICA DE PRIMER PASO
Dr. Hans Bowles
1. RADIOFÁRMACO
- Solución de sestamibi de tecnecio 199mTc](99M Tc-MIBI)
* Mecanismo de acción: complejo catiónico que difunde pasivamente a través de la membrana capilar y celular. Presenta afinidad por las proteínas citosólicas, localizándose en las mitocondrias y siendo su retención dependiente de la integridad de las mitocondrias reflejando los miocitos viables y el aumento del metabolismo dependiente de energía y la proliferación celular aumentada en diversas neoplasias. La localización en tiroides y paratiroides depende de la concentración de mitocondrias y la retención en los adenomas paratiroideos depende de la proporción de células oxifílicas.
- Solución de 99mTc-Tetrofosmina
* Mecanismo de acción: complejo lipofílico catiónico que difunde a través de la membrana celular. Presenta más afinidad por las proteínas citosólicas que el 99mTc-sestamibi acumulándose en el tejido miocárdico.
- Suspensión de 99mTc-hematíes marcados si a continuación ventriculografía en equilibrio
* Mecanismo de acción: la suspensión de 99mTc-hematíes permanecen en la circulación sanguínea con una semivida biológica de 80 días.
2. INDICACIONES
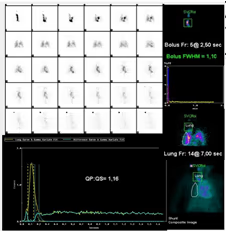
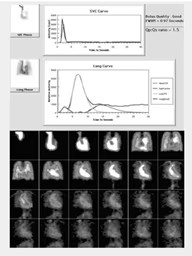
- Valoración y cuantificación de cortocircuitos izquierda-derecha.
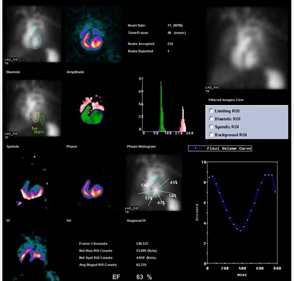
- Valoración de la función ventricular derecha e izquierda en reposo y en ejercicio: fracción de eyección, movimiento de la pared y otros parámetros sistólicos y diastólicos.
3. CONTRAINDICACIONES
- Embarazo
4. PROTOCOLO
4.1. Preparación del paciente
- Ninguna especial. No hace falta retirar medicación
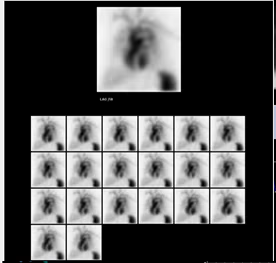
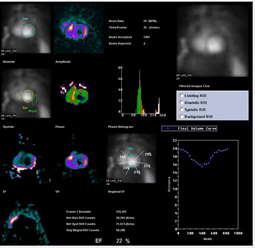
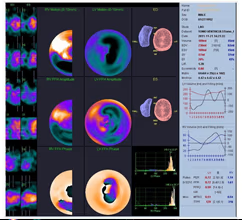
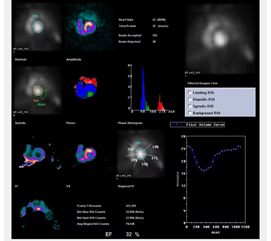
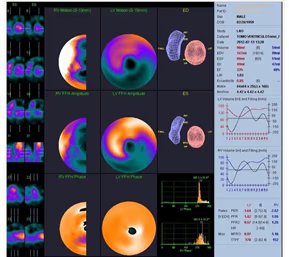
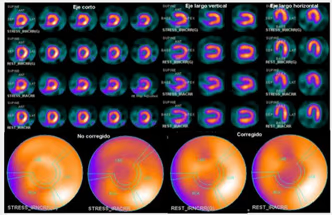
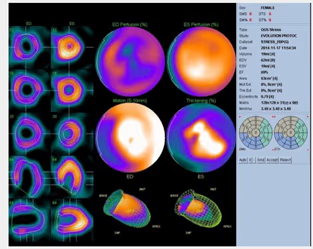
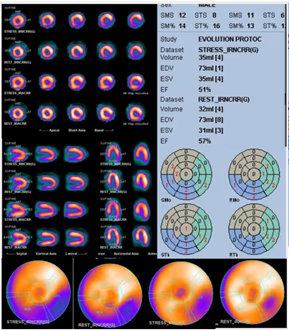
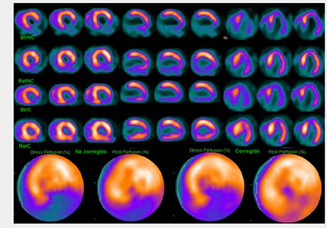
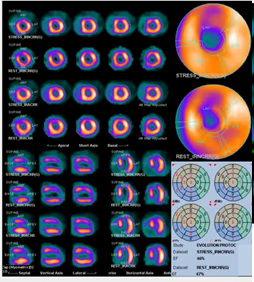
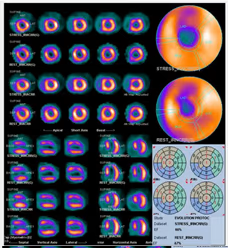
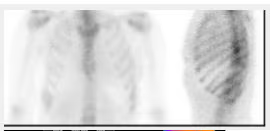
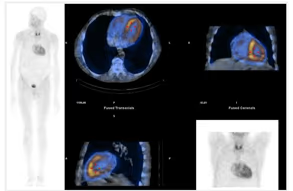
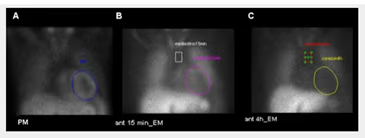
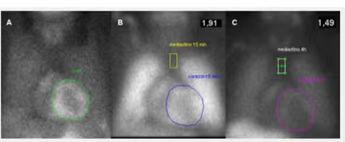
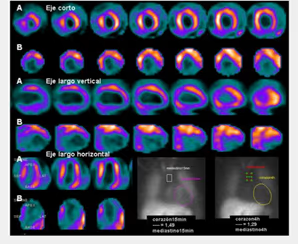
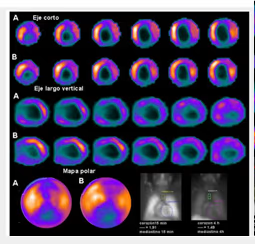
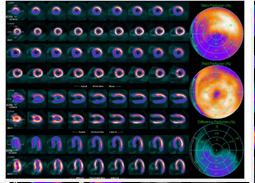
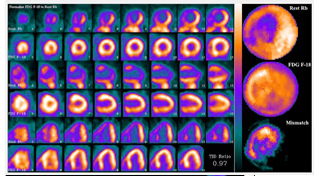
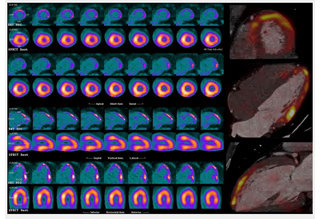
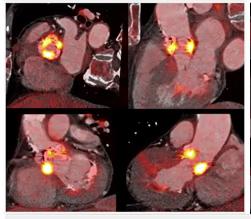
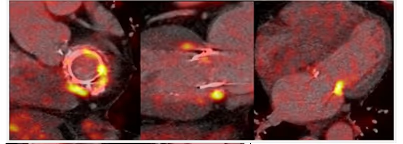
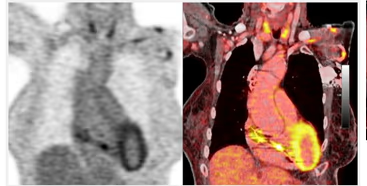
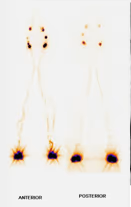
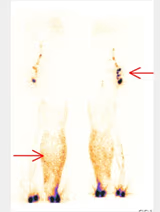
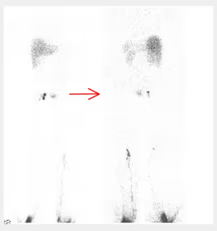
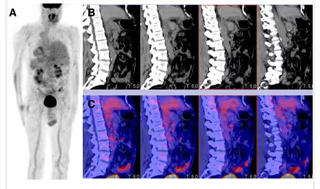
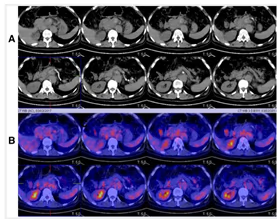
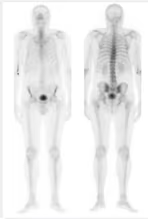
5. BIBLIOTECA DE IMÁGENES
- Imagen Normal