Gammagrafía Pulmonar de Perfusión
Dr. Hans Bowles
1. Radiofármaco
- Suspensión de macroagregados de albúmina de tecnecio (99mTc-MAA).
Mecanismo de acción:
La inyección intravenosa permite una microembolización de las arteriolas precapilares y capilares pulmonares (tamaño estándar entre 15 y 100 µm). El número estándar es de aproximadamente 400.000 partículas, permitiendo la obstrucción de una fracción muy pequeña del lecho vascular pulmonar.
2. Indicaciones
- Tromboembolismo pulmonar (TEP): diagnóstico inicial, seguimiento y respuesta al tratamiento.
- Evaluación de EPOC, enfisema y otras enfermedades obstructivas.
- Valoración de perfusión regional en malformaciones vasculares torácicas y cardiopatías congénitas.
- Distribución de perfusión en pulmón trasplantado.
- Cuantificación de perfusión pulmonar diferencial precirugía.
Nota: Para estudio de TEP se recomienda SPECT V/P.
3. Contraindicaciones
Relativas:
- Hipersensibilidad a seroalbúmina humana.
- Embarazo y lactancia.
Reducir número de partículas en:
- Hipertensión pulmonar, afectación vascular severa, cor pulmonale.
- Shunt derecha-izquierda (riesgo de depósito sistémico).
- Niños y embarazadas.
4. Protocolo
4.1 Preparación
- No requiere preparación específica del paciente.
- Disponer de Rx o TC de tórax de las 24 horas previas.
5. Biblioteca de Imágenes
- Imagen de perfusión normal: distribución homogénea de los MAA superponible a la radiografía de tórax (valorar la impresión hiliar, aórtica, costal o diafragmática) (Fig. 5).
- La gammagrafía pulmonar puede aportar información de otras patologías distintas del TEP.
- En EPOC los defectos de ventilación suelen ser mayores que los de perfusión (mismatch inverso).
- En casos de fallo cardíaco izquierdo la perfusión se redistribuye a segmentos superiores.
- La neumonía aparece como patrón coincidente en V/P siendo característico el signo de la cuerda ("stripe sign"), que es la perfusión mantenida en la periferia de un defecto coincidente central. También puede aparecer en casos de bullas, quistes, etc.
- Hay que comparar los hallazgos de una exploración con los de pruebas anteriores si existen (Figs. 6 y 7).
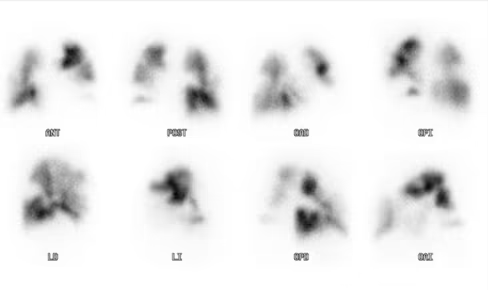
Fig. 1: 99mTc-MAA. Defectos de perfusión segmentarios, morfología triangular con base pleural.
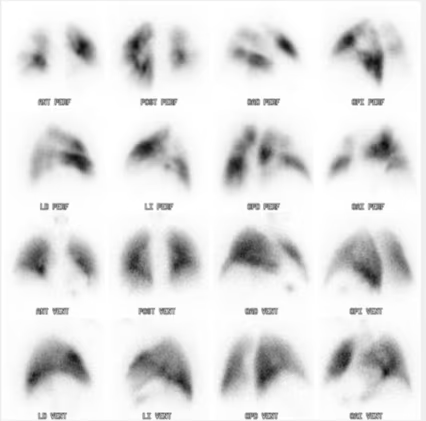
Fig. 2: Imágenes planares de perfusión pulmonar (99MTc-MAA, filas superiores) y de ventilación (filas inferiores) característico de TEP: Defectos de perfusión segmentarios con ventilación conservada.
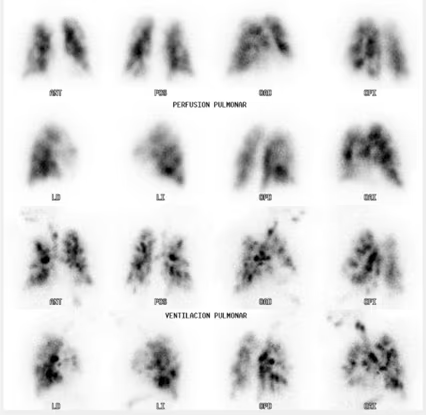
Fig. 3: Imágenes planares de perfusión pulmonar (99mTc-MAA, filas superiores) y de ventilación (filas inferiores). Utilidad en el seguimiento: TEP pre fibrinolisis.
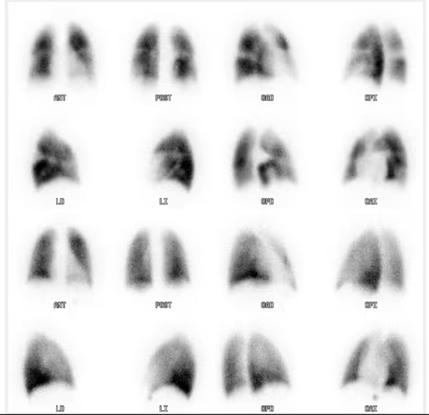
Fig. 4: Imágenes planares de perfusión pulmonar (99m Tc-MAA, filas superiores) y de ventilación (filas inferiores). Utilidad en el seguimiento TEP post fibrinolisis.
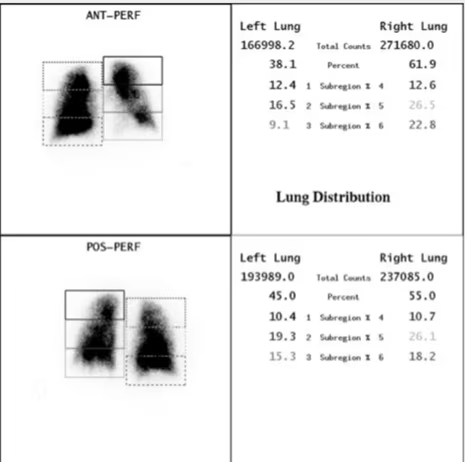
Fig. 5: Cuantificación de la Perfusión Pulmonar.
6. Informe al Clínico
- Datos del paciente y motivo de estudio.
- Antecedentes clínicos relevantes (TVP, cardiopatía, infecciones, tumores, radioterapia).
- Datos técnicos: radiofármaco, actividad y proyecciones.
- Descripción detallada de defectos (localización, forma, tamaño).
- Correlación con Rx y estudios previos.
- Impresión diagnóstica respondiendo la pregunta clínica.
GAMMAGRAFÍA DE VENTILACIÓN PULMONAR
Dr. Hans Bowles
1. Radiofármaco
- Aerosol de suspensión de carbono ultrafino marcado con pertecnetato (99mTc) de sodio, para ello se utiliza el equipo Technegas®
- Mecanismo de acción:
- Technegas® es un aerosol de partículas hidrofóbicas de carbono marcadas con 99mTc, con un diámetro entre 0.005-02 um. El tamaño de la partícula es tan pequeño que el aerosol se comporta como un gas hasta que llega a la periferia del pulmón donde las partículas son depositadas en bronquiolos y alveolos, sobre todo por difusión.
2. Indicaciones
- Complementar el estudio de perfusión en el diagnóstico del embolismo pulmonar.
- Cuantificación de la ventilación regional previa a cirugía torácica.
- Valoración de la distribución de la ventilación en el pulmón trasplantado
3. Contraindicaciones
- Relativas:
- Embarazo
- Lactancia
4. Protocolo
4.1 Preparación:
- Ninguna para el paciente, pero en casos de EPOC avanzada, puede ser útil administrar un broncodilatador para reducir los defectos de ventilación producidos por el broncoespasmo
- Disponer de radiografía o TC de tórax de las 24 horas previas a la gammagrafía.
- En pacientes con sospecha de TEP en que se haga ventilación y perfusión en protocolo de 1 día, realizar ANTES de la gammagrafía de perfusión.
- Es imprescindible la colaboración por parte del paciente que, con la nariz tapada, deberá inspirar por la boca el aerosol.
5. Biblioteca de Imágenes
- Imagen normal: distribución homogénea del radiofármaco (Fig. 3).
- Imagen anormal: distribución heterogénea del radiofármaco y/o defectos de ventilación (ausencia de captación) parcial o segmentaria (Fig. 4)
- Hay que tener en cuenta las alteraciones estructurales normales o acompañantes de la enfermedad: cardiomegalia, ensanchamiento mediastínico, derrames pleurales, modificaciones en el cayado aórtico y salida de los grandes vasos, etc.
La combinación de los estudios perfusión/ventilación muestra el territorio pulmonar embolizado como una zona segmentaria o parcialmente segmentaria con reducción o ausencia de la perfusión coincidente con una ventilación normal.

Fig. 1: Generador de Technegas
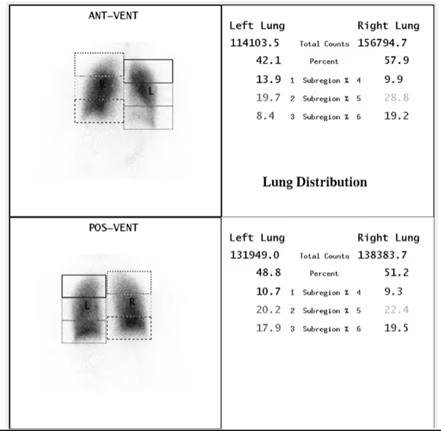
Fig. 2: Cuantificación de la Ventilación Pulmonar
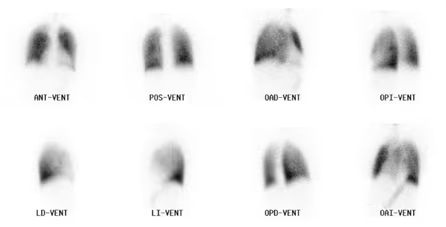
Fig. 3: Ventilación Normal.
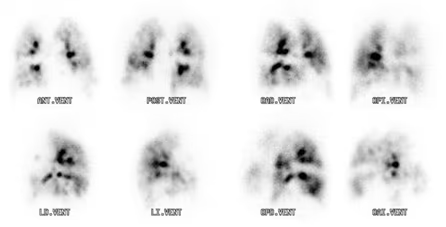
Fig. 4: Ventilación patológica con numerosos defectos de ventilación y acúmulos focales de actividad en árbol bronquial.
6. Informe al Clínico
- Datos del paciente y motivo de la exploración.
- Conocer siempre datos importantes de la historia clínica: trombosis venosa profunda, otras enfermedades pulmonares o cardíacas, infecciones, tumores o radioterapia pulmonar.
- Datos de la exploración: radiofármaco, actividad, proyecciones.
- Descripción de los hallazgos, siempre en relación con la radiografía y con la gammagrafía de perfusión: localización, forma y tamaño de los defectos de perfusión.
- Relacionar también con gammagrafías previas, si existen.
- Impresión diagnóstica que conteste a la pregunta clínica.
SPECT DE VENTILACIÓN / PERFUSIÓN PULMONAR
Dr. Hans Bowles
1. Radiofármaco
1.1 Ventilación
- Aerosol de suspensión de carbono ultrafino marcado con pertecnetato (99mTc) de sodio, para ello se utiliza el equipo Technegas
- Mecanismo de acción:
- Technegas es un aerosol de partículas hidrofóbicas de carbono marcadas con 99mTc, con un diámetro entre 0.005-02 um. El tamaño de la partícula es tan pequeño que el aerosol se comporta como un gas hasta que llega a la periferia del pulmón donde las partículas son depositadas en bronquiolos y alveolos, sobre todo por difusión.
1.2 Perfusión
- 99mTC-MAA
- Mecanismo de acción:
- La inyección i.v. permite una microembolización de las arteriolas precapilares y capilares (el tamaño estándar es entre 15 y 100 m). El número estándar de partículas es 400000, permitiendo una obstrucción de una muy pequeña fracción de vasos pulmonares.
- Es fundamental agitar el vial y jeringa de 99mTc-MAA antes de su administración, por la tendencia a sedimentarse. Además, no debe entrar sangre en la jeringa durante la administración, pues causa agregación de partículas de 99m Tc-MAA y puede ocasionar artefactos de "hotspots"
2. Indicaciones
- El SPECT es de elección según las guías EANM (sobre la gammagrafía planar), por su mayor sensibilidad, especificidad, reproducibilidad y un menor número de exploraciones no diagnósticas. Además, en caso de combinarse con un TC de baja dosis (SPECT-CT) mejora la especificidad.
- Presenta las siguientes INDICACIONES:
- Evaluar la probabilidad de tromboembolismo (TEP) agudo o crónico (la indicación más frecuente).
- De especial interés la HPTEC (Hipertensión pulmonar tromboembólica crónica) cuya incidencia es del 5% secundaria a TEP agudo, y en el que el SPECT V/P es la prueba de elección.
- De especial interés en el contexto de pandemia COVID-19, si sospecha de TEP por disnea persistente y alteración de la DLCO.
- Grado de resolución del embolismo pulmonar (estudios comparativos)
- Evaluar el trasplante pulmonar
- Detectar enfermedad cardíaca o pulmonar congénita (shunts cardíacos, estenosis de la arteria pulmonar, fístula A-V)
- Detectar la presencia de fístula bronco-pleural
- Evaluar enfermedades pulmonares crónicas (EPOC, fibrosis quística)
3. Contraindicaciones
- No hay contraindicaciones absolutas
3.1 Precauciones
- Utilizar la mitad de partículas (100000-200000) en estas situaciones:
- HTP conocida
- Shunt derecho-izquierdo
- Neumonectomía previa
- Trasplante pulmonar único
- Embarazo:
- En primer trimestre realizar gammagrafía de perfusión, y solo si es estrictamente necesario (perfusión no concluyente) completar con estudio de ventilación en protocolo de 2 días. Además, se aconseja reducir la actividad de 99mTc-MAA a 50 MBq
- Tras el primer trimestre, se puede considerar el estándar SPECT V/P
- Niños (reducir el número de partículas en función del peso)
- Lactancia: suprimirla durante 12 horas tras la administración del 99m Tc-MAA
4. Protocolo
4.1 Preparación y administración
- Disponer de Rx tórax en las 24 h previas al procedimiento para una mejor interpretación de la exploración
- Gammagrafía de ventilación
- Administración del 99MTc-Technegas con el paciente en decúbito supino o sentado
- Se administra por inhalación. El paciente con la nariz tapada debe inspirar el gas producido mediante una respiración profunda y lenta, seguida de una pausa de 5 segundos en la que aguante la respiración y a continuación expulsar el gas
- Repetir el proceso 2-3 veces
- Gammagrafía de perfusión
- Inyección lenta de bolo i.v. en 30 segundos
- Inyección en decúbito supino
- En caso de ortopnea, que esté lo más en decúbito que tolere
- Es fundamental disponer de Rx Tórax (o TC si existiese) en las 24 horas previas al estudio para una correcta interpretación de la exploración. En caso de disponer de un equipo SPECT-TC no precisaríamos de ese estudio previo de imagen morfológica
5. Biblioteca de Imágenes
Imagen Normal (Fig. 1a y 1b)
Visualizamos adecuada distribución del radiofármaco en ambos pulmones, sin observar alteraciones, tanto en el estudio de ventilación como en perfusión.
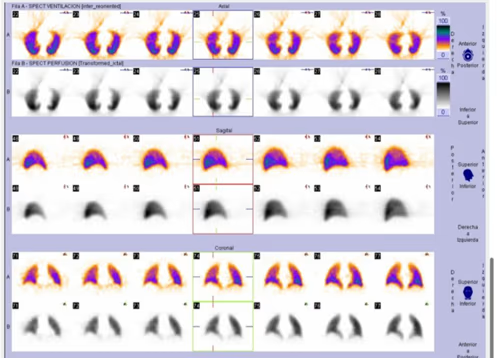
Fig. 1a. Estudio normal. Presentación de imágenes de ventilación y perfusión en las 3 proyecciones (axial, sagital y coronal). Cortes de 4.67 mm de grosor.

Fig. 1b. Estudio normal. Imágenes de ventilación, perfusión y perfusión sustraída en proyección coronal. Cortes sumados de 9.34 mm de grosor.
Imagen Patológica 1 (Fig. 2a, 2b y 2c)
Visualizamos tres defectos de perfusión subsegmentarios con ventilación conservada, correspondiente a tromboembolismo pulmonar.
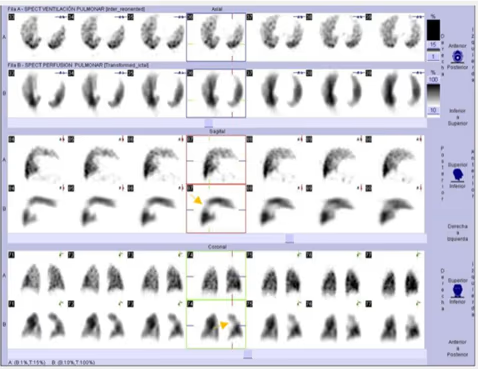
Fig. 2a. Estudio patológico. Presentación de imágenes de ventilación y perfusión en las tres proyecciones (axial, sagital y coronal). Se visualizan 3 defectos subsegmentarios en pulmón izquierdo en el estudio de perfusión, con ventilación conservada.
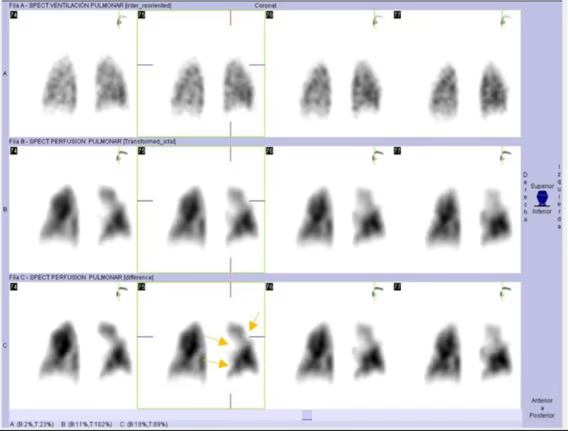
Fig. 2b. Estudio patológico. Imágenes de ventilación, perfusión y perfusión sustraída. Detalle de los defectos subsegmentarios del pulmón izquierdo en proyección coronal.
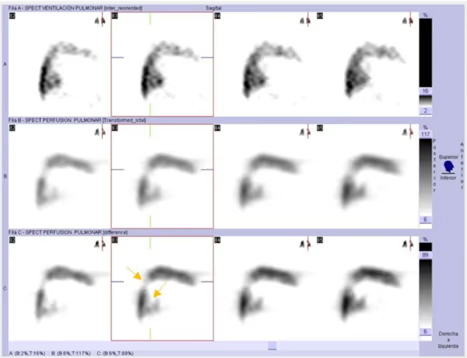
Fig. 2c. Estudio patológico. Imágenes de ventilación, perfusión y perfusión sustraída. Detalle de los defectos subsegmentarios del pulmón izquierdo en proyección sagital.
Imagen Patológica 2 (Fig. 3a, 3b, 3c y 3d)
Visualizamos dos defectos de perfusión segmentarios con ventilación conservada, diagnosticándose tromboembolismo pulmonar.
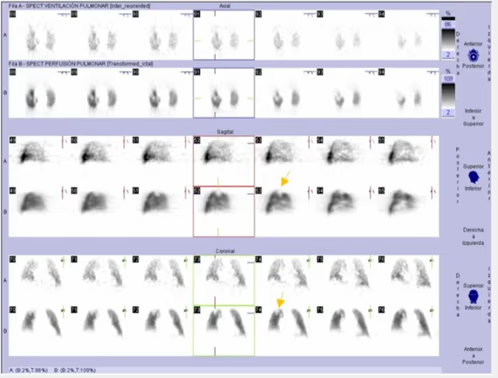
Fig. 3a. Estudio patológico. Presentación de imágenes de ventilación y perfusión en las tres proyecciones (axial, sagital y coronal). Se visualiza defecto segmentario en segmento posterior del LSD.
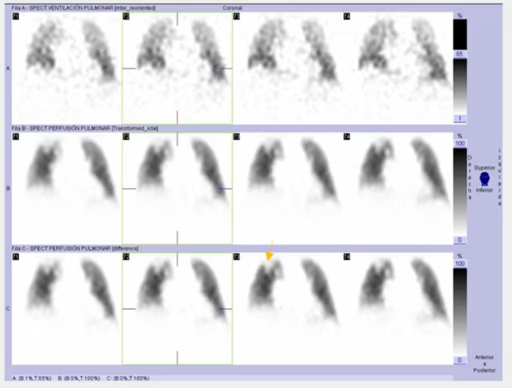
Fig. 3b. Estudio patológico. Imágenes de ventilación, perfusión y perfusión sustraída. Detalle del defecto segmentario en segmento posterior del LSD en proyección coronal.
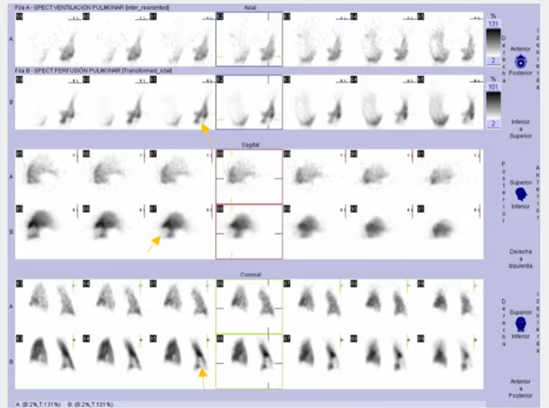
Fig. 3c. Estudio patológico. Presentación de imágenes de ventilación y perfusión en las tres proyecciones (axial, sagital y coronal). Se visualiza defecto segmentario en segmento postero-basal del LII.
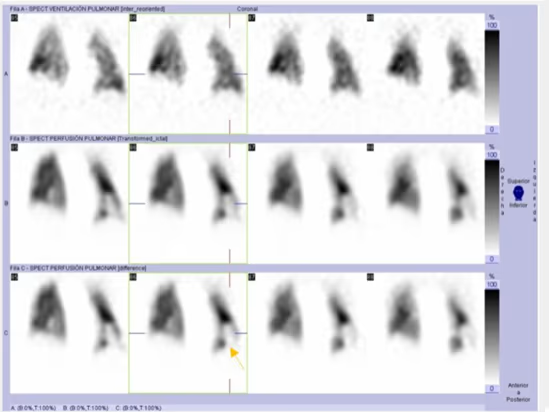
Fig. 3d. Estudio patológico. Imágenes de ventilación, perfusión y perfusión sustraída. Detalle del defecto segmentario en segmento postero-basal del LII en proyección coronal.
6. Informe al Clínico
- Describir los hallazgos
- Realizar una interpretación trinaria del estudio, según recomendación de la EANM 2019.
- Se ha de evitar informes basados en criterios probabilísticos (PIOPED 1), dado que muestran altas tasas de informes no diagnósticos.
- Hay que referir:
- Presencia de TEP:
- Discordancia V/P de al menos 1 segmento o 2 subsegmentos (defecto de perfusión de base pleural que delimite un segmento o subsegmento vascular con ventilación conservada)
- Ausencia de TEP:
- Patrón de perfusión normal
- Concordancia o discordancia inversa V/P (defectos de ventilación pero no de perfusión)
- Discordancia que no tiene patrón lobar, segmentario o subsegmentario
- Gammagrafía no diagnóstica
- Múltiples anormalidades de V/P no clasificables en los dos puntos anteriores
- Presencia de TEP:
DETECCIÓN DE FÍSTULA PERITONEO-PLEURAL
Dr. Hans Bowles
1. RADIOFÁRMACO
- Se puede utilizar 99mTc-DTPA, 99mTc-MAA o 99M Tc-nanocoloides de albúmina.
- No hay aprobación de ninguno de estos radiofármacos para esta indicación, por lo que el radiofármaco precisa ser solicitado mediante uso fuera de indicación de acuerdo a legislación española.
Mecanismo de acción:
- En el caso del 99MTC-DTPA tras su administración intraperitoneal, se distribuye en el espacio peritoneal mediante un mecanismo de difusión pasiva.
2. INDICACIONES
- Sospecha de fístula peritoneo-pleural en paciente que se encuentra en tratamiento con diálisis peritoneal (DP).
3. CONTRAINDICACIONES
- Embarazo
4. PROTOCOLO
4.1 Preparación
- Disponer de Rx tórax en las 24 h previas al procedimiento
- Reducir el derrame pleural
- Toracocentesis en caso de derrame pleural masivo
- Realizar la exploración lo más espaciada posible de la DP previa (para reducir la presión hidrostática en la cavidad pleural)
- Disponer del equipo para la realización de DP en el servicio de medicina nuclear
- Contar con la colaboración del nefrólogo o enfermería de diálisis
5. BIBLIOTECA DE IMÁGENES
Imagen normal: ausencia de fístula peritoneo-pleural (Fig. 1, 2 y 3)
Depósito del radiofármaco en cavidad peritoneal, sin observarse paso a cavidad pleural en las distintas fases del estudio, en paciente con derrame pleural izquierdo.
Fig.1. Rx tórax realizada en las 24 h previas. Derrame pleural izquierdo a estudio en paciente con diálisis peritoneal
Fig.2. Estudio dinámico. Tras realizar la diálisis peritoneal con el fluido dializador radiomarcado se inicia estudio dinámico precoz. Se obtienen 30 imágenes de 30 segundos cada una, sin observarse paso a cavidad pleural, únicamente captación abdominal
Fig.3. Estudio estático. (A) Imágenes de tórax a los 45 min y (B) tardías a las 2 horas, sin visualizarse paso de actividad a cavidad pleural, y observándose elevación diafragmática derecha ya conocida; se descarta la fístula peritoneo-pleural
Imagen patológica (Fig. 4,5 y 6)
Paso del radiofármaco de cavidad peritoneal a cavidad pleural, visualizándose depósito en cavidad pleural, siendo demostrativo de fístula peritoneo-pleural.
El depósito puede verse ya desde el estudio dinámico, aunque en función de las presiones hidrostáticas y del calibre de la comunicación la visualización puede ser más precoz o tardía.
Fig.4. Rx tórax realizada en las 24 h previas. (A) Derrame pleural derecho a estudio en paciente con diálisis peritoneal. Ante sospecha de fístula peritoneo-pleural se suspendió la diálisis peritoneal tres días y se realizó nuevo control (B) que muestra reducción del derrame pleural Se recomienda realizar toracocentesis previa en caso de derrame pleural masivo y realizar la exploración lo más espaciada posible de la DP previa, para reducir la presión hidrostática en la cavidad pleural y facilitar la detección
Fig.5. Estudio dinámico. Tras realizar la diálisis peritoneal con el fluido dializador radiomarcado se inicia estudio dinámico precoz. Se obtienen 30 imágenes de 30 segundos cada una, observándose paso de actividad a cavidad pleural derecha desde la primera imagen de la adquisición
Fig.6. Estudio estático. (A) Imágenes de tórax a los 45 min y (B) tardías a las 2 horas, visualizando paso de actividad a cavidad pleural derecha, confirmando la fístula peritoneo-pleural.
6. INFORME AL CLÍNICO
- Describir motivo de la exploración y sintomatología del paciente
- Describir los hallazgos:
- Indicar si es o no patológico el estudio
- Indicar la lateralidad (si es comunicación derecha o izquierda)
- Es fundamental indicar en qué momento se inicia la visualización del paso del radiofármaco a cavidad pleural (si es ya desde el estudio dinámico inmediato o es más tardío)
- Puede tener repercusión en la elección del manejo terapéutico (hemodiálisis temporal esperando la cicatrización espontánea, hemodiálisis temporal mientras se realiza reparación quirúrgica, o bien, hemodiálisis definitiva)
PET-TC EN CÁNCER DE PULMÓN
Dr. Hans Bowles
1. RADIOFÁRMACO
- Solución de Fluordesoxiglucosa (18F-FDG)
Mecanismo de acción: incorporación a las células que utilizan glucosa como fuente primaria de energía, mediante un transportador tisular insulinodependiente que se acumula en tejidos que presentan aumento de la glicolisis
2. INDICACIONES
2.1 Caracterización del nódulo pulmonar solitario (NPS):
- Útil en diagnóstico diferencial benignidad/malignidad de nódulos indeterminados, especialmente cuando son > 8mm; y para determinar el lugar óptimo de biopsia, sobre todo cuando se trata de lesiones heterogéneas.
2.2 Estadificación TNM:
- Evalúa actividad de la lesión, estado ganglionar y metástasis.
T: Utilidad si atelectasia o derrame pleural. La infiltración mediastínica y de pared torácica se visualiza mejor con CT diagnóstico y contraste i.v.
A los nódulos en vidrio deslustrado sugestivos de malignidad se les da un valor de la T en función de la extensión del componente sólido en CT.
N: El PET es más sensible para la evaluación de adenopatías que el CT. Las adenopatías hipermetabólicas guían el EBUS para su filiación anatomopatológica. Es de especial interés cuando la presencia de adenopatías afectas cambia el estadiaje y supone una contraindicación a la cirugía curativa.
M: Detección de metástasis.
2.3 Evaluación de eficacia tras el tratamiento
- Ayuda al diagnóstico diferencial de cambios post radioterapia vs recidiva/persistencia.
Existen limitaciones para la valoración con PET cuando existen metástasis cerebrales (mejor valoración mediante RM); cuando aparecen lesiones granulomatosas o infecciosas con actividad inflamatoria reactiva; cuando se trata de nódulos subcentimétricos, tumores mucinosos o tumores con baja avidez por la FDG; cuando hay invasión de la pared torácica.
3. CONTRAINDICACIONES
- Embarazo: no es contraindicación absoluta, a valorar riesgo-beneficio.
- Lactancia: no hace falta interrumpirla, pero se recomienda limitar contacto físico 12 horas tras la inyección de la 18F-FDG.
4. PROTOCOLO
Para más información ver PET TC: procedimiento, imagen normal y variantes.
4.1 Preparación del paciente
- Si lesión cercana al corazón, se recomienda dieta baja en hidratos de carbono 48 h, ayunas de al menos 6 h y opcional protocolo de frenación con heparina.
5. BIBLIOTECA DE IMÁGENES
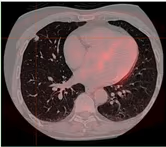
Fig. 1 Imagen transversal de fusión PET-TC en ventana de pulmón con NPS ametabólico en LM, sugestivo de benignidad.
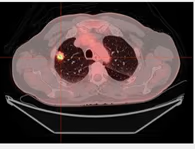
Fig. 2 Imagen transversa de fusión PET-TC en ventana de pulmón con NPS hipermetabólico en LSD, sugestivo de malignidad
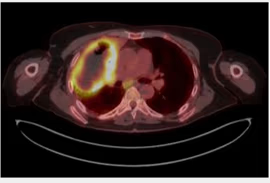
Fig. 3: Corte axial de PET-TC. Masa cavitada en lóbulo superior de pulmón derecho, de bordes irregulares hipermetabólicos, con necrosis central, sugestiva de malignidad. Presenta amplio contacto con pleura, tanto en la región de pared como a nivel mediastínico y obstruye el bronquio lobar superior derecho. Presenta aire en el interior de la zona necrótica, a valorar clínicamente la posibilidad de fístula traqueo-bronquial.
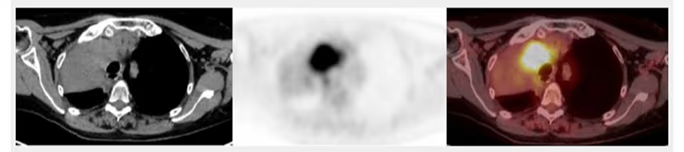
Fig. 4 Cortes transversales de CT, PET y PET-TC donde se diferencia lesión pulmonar de zona de atelectasia
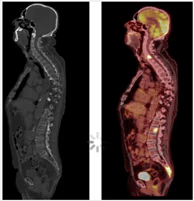
Fig. 5 Cortes sagitales de TC y PET-TC. La imagen molecular permite detectar lesiones que no son todavía visibles en la imagen morfológica, en este caso metástasis a nivel óseo (M1c)
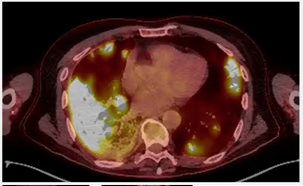
Fig. 6 Imagen axial de PET-TC en paciente con tumor de crecimiento neumónico, no medible, con afectación de todo un lóbulo, en este caso el lóbulo inferior de pulmón derecho (T3) con lesiones pleurales múltiples homo y contralaterales en relación con metástasis (M1a).
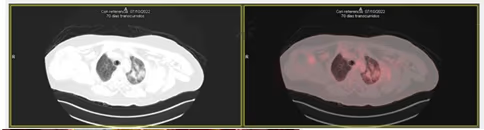
Fig. 7 Imágenes axiales de TC y de fusión PET-TC con leve hipermetabolismo en área de neumonitis post-rádica en lóbulo superior de pulmón izquierdo, sin focos de intenso hipermetabolismo que sugieran recidiva tumoral.
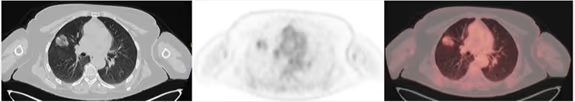
Fig. 8 Imágenes transversas de CT, PET y PET-TC en paciente con opacidad en vidrio deslustrado > 3 cm con polo sólido de 1.5 cm en lóbulo superior de pulmón derecho (T1b).
6. INFORME AL CLÍNICO
- Datos del paciente y motivo de consulta.
- Datos de la técnica de exploración: radiofármaco, actividad, tiempo de adquisición, campos adicionales.
- Descripción sistemática combinada PET y TC por localización anatómica y por orden de importancia de los hallazgos.
- Impresión diagnóstica clara y concisa que responda a la pregunta clínica. Si no fuese posible, se pueden sugerir diagnósticos diferenciales y técnicas complementarias.
ESTUDIO DEL ACLARAMIENTO MUCO-CILIAR
Dr. Hans Bowles
1. RADIOFÁRMACO
- 99M Tc-macroagregados de albúmina
Mecanismo: La suspensión de macroagregados de albúmina migra por transporte mucociliar.
2. INDICACIONES
- Sospecha alteración del transporte mucociliar
- Infecciones respiratorias de repetición
- Sospecha de síndrome de discinesia ciliar primaria.
3. CONTRAINDICACIONES
- No existen contraindicaciones absolutas.
4. PROTOCOLO
4.1 Preparación del Paciente
- El procedimiento no debe realizarse si el niño presenta una infección respiratoria (esperar 4-6 semanas).
5. BIBLIOTECA DE IMÁGENES
Imagen normal
Estudio dinámico que muestra captación inicial tras instilar el radiofármaco y adecuado transporte mucociliar a lo largo del estudio (Fig. 1)
Imagen Patológica
Estudio dinámico que muestra ausencia de transporte mucociliar. (Fig. 1)
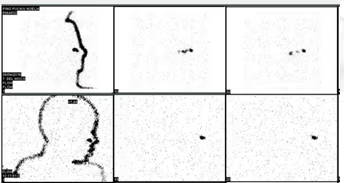
Fig.1
99mTc-MAA. Imagen lateral de cabeza a 1, 10 y 20 minutos tras la instilación del radiofármaco. Fila superior: estudio normal, migración de los MAA (4.14 ml/min). Fila inferior: estudio patológico, ausencia de migración de los MAA
6. INFORME AL CLÍNICO
- Datos del paciente y motivo de la exploración.
- Información clínica relevante (incluyendo antecedentes respiratorios del paciente).
- Parámetros técnicos (actividad, procedimiento)
- Descripción de los hallazgos: describir si se ha producido captación indicativa de transporte mucociliar y la velocidad calculada.
- Conclusión diagnóstica
ANATOMÍA DEL TÓRAX. LA IMAGEN TC
Dr. Hans Bowles
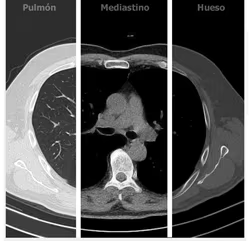
Para el estudio detallado del TC torácico es de utilidad realizar una división en 3 áreas o zonas que se evaluarán con diferentes niveles de ventana: pulmón, mediastino y pared torácica.
Es recomendable seguir de forma rutinaria un orden de evaluación de las estructuras con el fin de no pasar por alto hallazgos relevantes. Las reconstrucciones multiplanares son útiles en la localización de lesiones e identificación de estructuras.
- Pulmón: Ventana de pulmón (centro -500 UH y anchura 150-200 UH). Permite identificar la macroestructura del parénquima pulmonar, bronquios y cisuras, así como delimitar lesiones focales o alteraciones estructurales.
- Mediastino y tejidos blandos: Ventana de mediastino (centro 50 UH y anchura 350 UH). Permite identificar estructuras mediastínicas y adenopatías mediastínicas, supraclaviculares y axilares. La administración de contraste intravenoso iodado incrementa la resolución de contraste y facilita la identificación de realces anómalos inflamatorios o neoplásicos.
- Pared torácica ósea: Ventana ósea (centro 300 UH y anchura 1500 UH).
Permite evaluar y caracterizar anomalías o lesiones focales en la parrilla costal y las vértebras.
Parénquima, cisuras, lóbulos y segmentos pulmonares
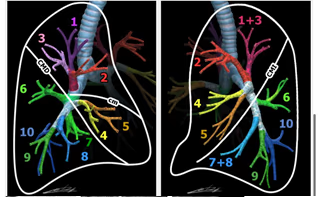
Bronquios lobares y segmentarios. Nótese las diferencias del pulmón izquierdo respecto al derecho: Los segmentos 1 y 3, así como 7 y 8 izquierdos, están fusionados. La disposición de los segmentos 4 y 5 en el pulmón derecho es horizontal, correspondientes al lóbulo medio, mientras que en el pulmón izquierdo es vertical, correspondientes a la língula.
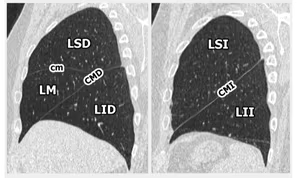
Reconstrucciones sagitales del parénquima pulmonar, permiten identificar fácilmente la disposición de las cisuras y los lóbulos pulmonares.
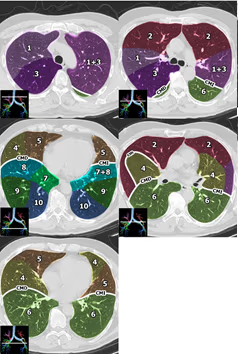
LSD: Lóbulo superior derecho, LM: Lóbulo medio, LID: Lóbulo inferior derecho, CMD: Cisura mayor derecha, cm: Cisura menor, LSI: Lóbulo superior izquierdo, LII: Lóbulo inferior izquierdo
Segmentos del pulmón derecho: 1 Apical del LSD, 2 Anterior del LSD, 3 Posterior del LSD, 4 Lateral del LM, 5 Medial del LM, 6 Apical del LID, 7 Basal medial, 8 Basal anterior, 9 Basal lateral, 10 Basal posterior.
Segmentos del pulmón derecho: 1+ 3 Apicoposterior del LSI, 2 Anterior del LSI, 4 Superior de la língula, 5 Inferior de la língula, 6 Apical del LII, 7+8 Basal anteromedial, 9 Basal lateral, 10 Basal posterior.
Estructuras anatómicas del mediastino.
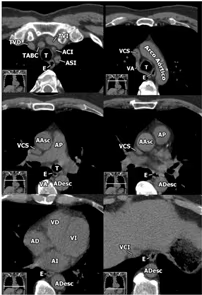
T: Tráquea, E: Esófago, TVD: Tronco venoso derecho, TVI: Tronco venoso izquierdo, ACI: Arteria carótida interna, ASI: Arteria subclavia izquierda, TABC: tronco arterial braquiocefálico, AAsc: Aorta ascendente, ADesc: Aorta descendente, AP: Arteria pulmonar, VA: Vena ácigos, VCS: Vena cava superior, VCI: Vena cava inferior, AD: Aurícula derecha, AI: Aurícula izquierda, VD: Ventrículo derecho, VI: Ventrículo izquierdo
Estaciones ganglionares
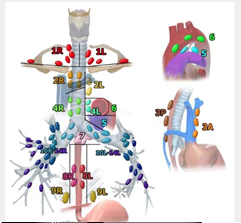
* Ganglios supraclaviculares
Ganglios supraclaviculares
- 1R y 1L: Cervicales bajos, supraclaviculares y ganglios de la escotadura supraesternal
Ganglios mediastínicos superiores
- 2R y 2L: Paratraqueales altos
- 4R y 4L: Paratraqueales bajos
- El límite de separación entre paratraqueales altos y bajos derechos corresponde al borde inferior del tronco venoso braquiocefálico izquierdo. En los izquierdos corresponde al borde superior del arco aórtico.
- Los ganglios pretraqueales se consideran dentro del grupo derecho (R).
- 3A y 3P: Prevasculares y prevertebrales
Ganglios aórticos
- 5: Ventana aortopulmonar
- 6: Para-aórticos
Ganglios mediastínicos inferiores
- 7: Subcarinales
- 8: Paraesofágicos
- 9: Ganglios de los ligamentos pulmonares
10-14: Ganglios hiliares, interlobares, lobares, segmentarios y subsegmentarios.