PET-TC. PROCEDIMIENTO, IMAGEN NORMAL Y VARIANTES
Dr. Hans Bowles
1. Radiofármaco
- Solución de fluordesoxiglucosa [18F] - FDG
- Mecanismo de acción: incorporación a la célula mediante un transportador tisular insulinodependiente. Atrapamiento metabólico en las células que utilizan glucosa como fuente primaria de energía, acumulándose en tejidos con aumento de la glicólisis.
2. Indicaciones
- Estadificación de pacientes con neoplasias malignas conocidas.
- Diferenciación de lesiones benignas de malignas.
- Búsqueda de un tumor primario desconocido cuando la enfermedad metastásica es la primera manifestación del cáncer o en síndromes paraneoplásicos.
- Evaluar el efecto de la terapia en tumores malignos conocidos.
- Determinar si las anomalías residuales detectadas en la exploración física o en otros estudios de imagen tras el tratamiento representan fibrosis o necrosis.
- Detectar la recidiva tumoral, especialmente en presencia de marcadores tumorales elevados.
- Selección de la región del tumor con mayor probabilidad de aportar información diagnóstica para la biopsia.
- Orientar la planificación de la radioterapia.
- Valoración del metabolismo cerebral cortical en TCE.
- Enfermedades neurodegenerativas.
- Actividad en procesos infecciosos -inflamatorios (vasculitis, infecciones valvulares, etc.).
- Valoración de la viabilidad miocárdica.
3. Contraindicaciones
- Embarazo:
- Valorar riesgo - beneficio.
- Lactancia:
- Limitar contacto 12 horas después de la inyección. No es preciso interrumpir la lactancia tras la administración de FDG ya que se excreta poco radiofármaco en la leche. Sin embargo, como la mama acumula FDG se recomienda que se limite el contacto entre la madre y el niño.
4. Protocolo
4.1 Preparación del paciente
- Ayunas de al menos 4 h. La nutrición parenteral debe suspenderse también 4 h antes de la inyección de FDG.
- Hidratación con agua 2 horas antes (500 - 1000 mL).
- No ejercicio físico como mínimo 6h antes (preferible 24 horas previas), evitar masticar chicles en especial en tumores de cabeza-cuello.
- Evitar frío para impedir la activación de la grasa parda, así como intentar que el paciente esté en un lugar cálido y tranquilo al menos durante 30-60min antes de la inyección del radiofármaco.
- Si es necesaria sedación, administrar el RF antes de la misma.
- Si lesión cercana o en corazón, se recomienda dieta baja en hidratos de carbono y rica en grasas durante al menos 24 h y ayunas de 6 - 12 h. Además, se puede incorporar un protocolo de frenación de captación miocárdica con heparina, que consiste en administrar una dosis de 50 Ul/kg de heparina sódica endovenosa 15 minutos antes de la 18F-FDG.
- No es necesario retirar medicación, aunque en estudios de cuantificación se ha de evitar el tratamiento con corticoides las 2 semanas previas.
- En pacientes diabéticos:
- Tipo 1: en caso de mal control diabético, inyectar su insulina según protocolo habitual y esperar 4 - 6 h antes de la inyección de la FDG.
- Tipo 2: toma de medicación antidiabética habitual, manteniendo el ayuno e inyectar la FDG 4-6 h después.
- Determinación de la glucemia: si es mayor de 200 mg/dL, no se debe realizar el PET. Se recomienda normalizar la glucemia y realizar la exploración otro día. La hiperglucemia disminuye la captación del radiofármaco en las lesiones y el hiperinsulinismo produce un aumento del depósito muscular de 18F-FDG.
- Diazepam: puede administrarse v.o. para ayudar en la relajación de los pacientes antes de la prueba. No recomendado en timomas por riesgo de crisis miasténica.
- Si contraste i.v, valorar riesgo de nefrotoxicidad (> 60 años, nefropatía, DM, HTA, metformina). Si nefropatía, usar contraste iso-osmolar, hidratación, retirar AINEs, diuréticos, metformina y aminoglucósidos. No realizar otra prueba con contraste durante 72 h. Se recomienda no reintroducir metformina hasta 48 h después del contraste yodado i.v. si factores de riesgo de nefrotoxicidad
5. Biblioteca de Imágenes
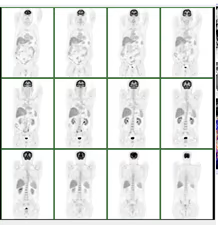
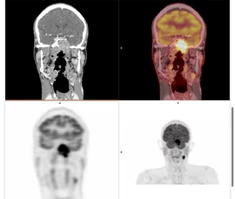
Fig. 1: Imagen 18F-FDG normal de cuerpo completo. Cortes coronales.
Cerebro:
- Intenso hipermetabolismo en la sustancia gris cortical y subcortical con sustancia blanca hipometabólica.
- Nervio óptico y músculos oculares extrínsecos hipermeabólicos.
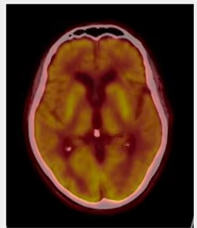
Fig. 2: Imagen transversal de fusión PET-TC cerebral con captación normal en sustancia gris cortical y subcortical. Calcificaciones en plexos coroideos y glándula pineal.
Cabeza y cuello
- Hipermetabolismo intenso y simétrico en anillo de Waldeyer.
- Discreto hipermetabolismo simétrico en salivares.
- Cuerdas vocales: hiper o ametabólicas en función de su uso en la distribución del RF; si asimetrías o parálisis N. Laríngeo Recurrente con ametabolismol en el lado enfermo.
- Tiroides: metabolismo variable tanto en tiroides normal como en patológico. Hipermetabolismo difuso y simétrico en enfermedad de Graves y tiroiditis, y focal y asimétrico en patología nodular.
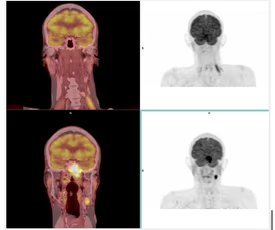
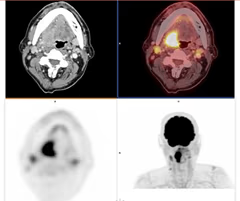
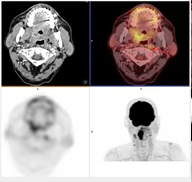
- Puede existir hipermetabolismo fisiológico en grasa parda y musculatura cervical (Fig. 4), así como secundario a cambios inflamatorios e infecciosos (Fig. 5).
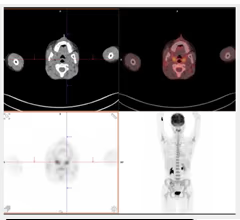
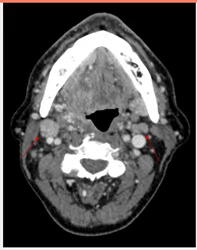
Fig. 3: Cortes axiales y MIP. Se observa captación fisiológica en amígdalas palatinas
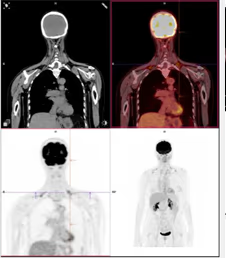
Fig. 4: Cortes coronales e imagen MIP con hipermetabolismo en grasa parda
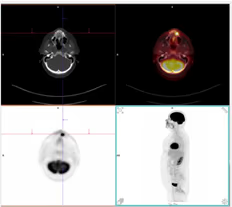
Fig. 5: Cortes transversales y MIP donde aparece hipermetabolismo focal en maxilar superior secundario a proceso dental.
Tórax
- Metabolismo cardiaco: variable, más intenso en ventrículo izquierdo y músculos papilares (Fig. 6).
- Mediastino: sirve de patrón de referencia para valoración cualitativa de las lesiones.
- Hipermetabolismo pulmonar si la imagen no está corregida por atenuación. Hipometabolismo si se realiza corrección de la atenuación.
- Timo (Fig. 7): es normal verlo en pacientes jóvenes o con factores estimulantes de colonias granulocíticas.
- Mama y pezón: HM en lactantes y hormonoterapia.
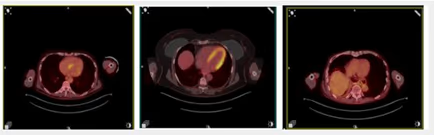
Fig. 6: Imágenes transversales de fusión PET-TC con diferentes patrones de metabolismo miocárdico, todos ellos normales: Captación parcheada heterogénea (izquierda); captación miocárdica en ventrículo izquierdo (centro); ausencia de captación miocárdica (derecha)
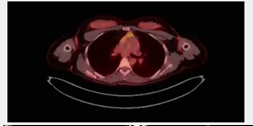
Fig. 7: PET-TC: corte trasversal de tórax con hipermetabolismo en timo.
Abdomen
- Pared gástrica: hipermetabólica (signo del Donought).
- Hipermetabolismo focal leve en cardias y píloro.
- Hipermetabolismo duodenal puede ser fisiológico.
- Metabolismo hepático que disminuye si imagen tardía. Suele ser patrón de referencia para comparación cualitativa con bazo y suprarrenales.
- La I8F-FDG no se excreta por la bilis. Cualquier foco HM en vesícula o árbol biliar obliga a descartar malignidad.
- Eliminación intestinal de 18FDG variable.
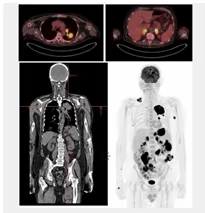
- Patrón focal (Fig. 8): maligno (tumor) o benigno (pólipos). Recomendar colonoscopia.
- Patrón segmentario: actividad inflamatoria.
- Patrón difuso (Fig. 9): post-QMT, DMNID
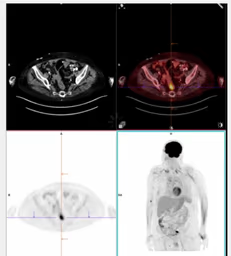
Fig. 8: Cortes transversales y MIP con lesión focal hipermetabólica en sigma de la que se aconseja estudio dirigido (colonoscopia).
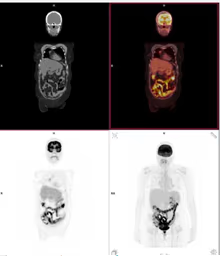
Fig. 9: Cortes coronales y MIP con hipermetabolismo intestinal difuso secundario a la toma de antidiabéticos orales
Pelvis
- HM ovárico en ovulación. En mujeres post-menopausicas, el HM ovárico obliga a descartar malignidad. HM endometrial en menstruación.
- Testículos: captación difusa, homogénea y simétrica.
- Miembros y musculoesquelético:
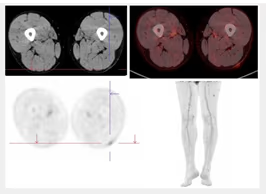
- Leve hipermetabolismo muscular, intenso si ejercicio físico (Fig. 10).
- Hipermetabolismo si expansión de médula ósea visible en región proximal de huesos la columna (Fig. 11).
- Fracturas: hipermetabolismo visible durante al menos 3 meses.
- Patología articular, prótesis (Fig. 11 y 12).
- Ercarmaiento prolongado ihipermetabolismo muscular).
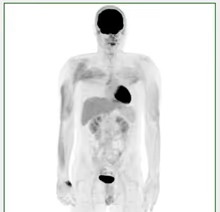
Fig. 10: Imagen MIP con hipermetabolismo muscular en miembros superiores y pared torácica por ejercicio físico
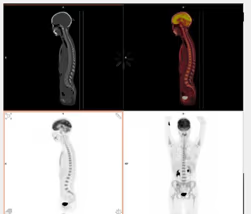
Fig. 11: Imágenes de CT, PET, fusión PET-TC y MIP con hipermetabolismo difuso óseo en vértebras y región proximal de huesos largos, en relación con hiperplasia médula ósea.
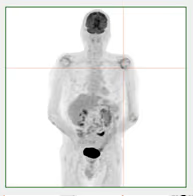
Fig. 12: Imagen MIP con hipermetabolismo en articulaciones glenohumerales.
Artefactos debidos a la TC (mapas de atenuación):
- Contraste: la alta densidad del contraste i.v. produce falsas imágenes hipermetabólicas en PET. En algunos equipos existe una corrección por software.
- Objetos metálicos (falso hipermetabolismo que desaparecen en la imagen no corregida por atenuación (Fig. 13)). En algunos equipos existe una corrección por software.
- Respiración/Movimiento (diafragma): desaparece al realizar estudio sincronizado con la respiración. Normalmente es válida una respiración relajada.
- Truncation: por la diferencia de tamaño del campo de visión entre la TC y la PET (normalmente mayor) (Fig. 14).
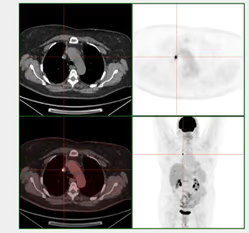
Fig. 13: Falso hipermetabolismo en vena cava superior por artefacto de hipercorrección.
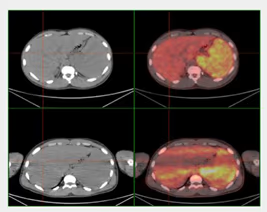
Fig. 14: Cortes transversales de TC y de fusión PET-TC. Artefacto de truncation (abajo) que desaparece al subir los brazos (arriba).
Debidos a la PET:
- Extravasación del radiofármaco en el punto de inyección (Fig. 15).
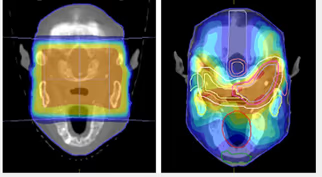
- Cambios en la imagen sin y con CA (Fig. 16).
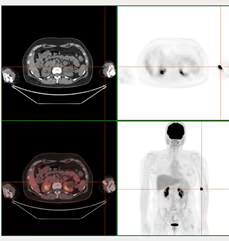
Fig. 15: Cortes transversales y MIP. Extravasación en el punto de inyección en flexura de codo izquierdo
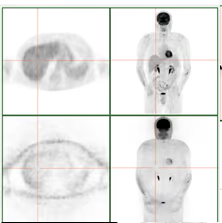
Fig. 16: Cortes transversales y MIP de imagen normal con (arriba) y sin (abajo) corrección de atenuación.
6. Informe al Clínico
- Datos del paciente y motivo de consulta.
- Datos de la técnica de exploración: trazador, actividad, tiempo de adquisición, campos adicionales.
- Descripción ordenada y completa de los hallazgos: se sugiere la descripción sistemática combinada PET y TC) por localización anatómica y por orden de importancia de los hallazgos en cada región: cabeza y cuello, tórax, abdomen y pelvis y músculo-esquelético.
- Impresión diagnóstica clara y concisa que responda a la pregunta clínica. Si no fuese posible, se pueden sugerir diagnósticos diferenciales y técnicas complementarias útiles al respecto.